心血管特异标记的转基因斑马鱼品系推荐
作者:zhangyun 发布时间:2020/6/22 4:00:00斑马鱼体型小,易于养殖,体外受精和发育,且早期胚胎透明,易于观察及操作,受精后24小时主要的组织器官原基已形成,是理想的实验动物。 斑马鱼胚胎可以靠被动扩散供氧生存相当长时间,因而具有严重心血管发育缺陷的胚胎也能够在早期发育中存活。这些优点使斑马鱼成为研究脊椎动物心血管发育和疾病的强大模型。荧光蛋白标记心血管系统的转基因斑马鱼品系也在心血管发育、疾病发生、损伤再生、肿瘤发生、癌细胞迁移等诸多研究中成为不可或缺的工具。
在脊椎动物中,心血管系统是胚胎发育中最早形成并行使功能的组织器官之一。 斑马鱼心脏发育大概分为以下几个阶段:最早于5hpf,中胚层前外侧板出现心脏的前体细胞;15hpf 左右心脏前体细胞向胚胎中线处融合并成心锥,然后向前延伸形成线性的心管;约22hpf心脏开始出现收缩;28hpf左右心房和心室形成;48hpf左右瓣膜形成,新房心室可清晰识别[1]。和高等脊椎动物一样,斑马鱼的血管原细胞也来源于中胚层,14-16hpf迁移至躯干中线部位并形成血管索。然后,血管原细胞分化形成成血管细胞和造血细胞。成血管细胞进一步分化形成轴向血管、背部主动脉和后主静脉,约24hpf 开始出现血液循环[2]。

图1 斑马鱼胚胎的心脏血管系统
国家斑马鱼资源中心多年来收集并保藏了多个心脏血管表达荧光蛋白的转基因品系,都已在中心网站发布,现做一归纳汇总,方便广大科研工作者更好的开展工作。 全部心血管标记的清单见文末,现就常用品系逐一进行介绍。
首先介绍心脏特异性标记的荧光品系。CZ56(f1Tg,Tg(myl7:eGFP))该品系为心肌细胞特异性表达基因myosin light chain 7(myl7)启动子调控绿色荧光蛋白(eGFP)在整个心脏肌肉细胞内表达(图2)[3]。 被广泛应用于各种心血管模型以及心脏疾病的研究。
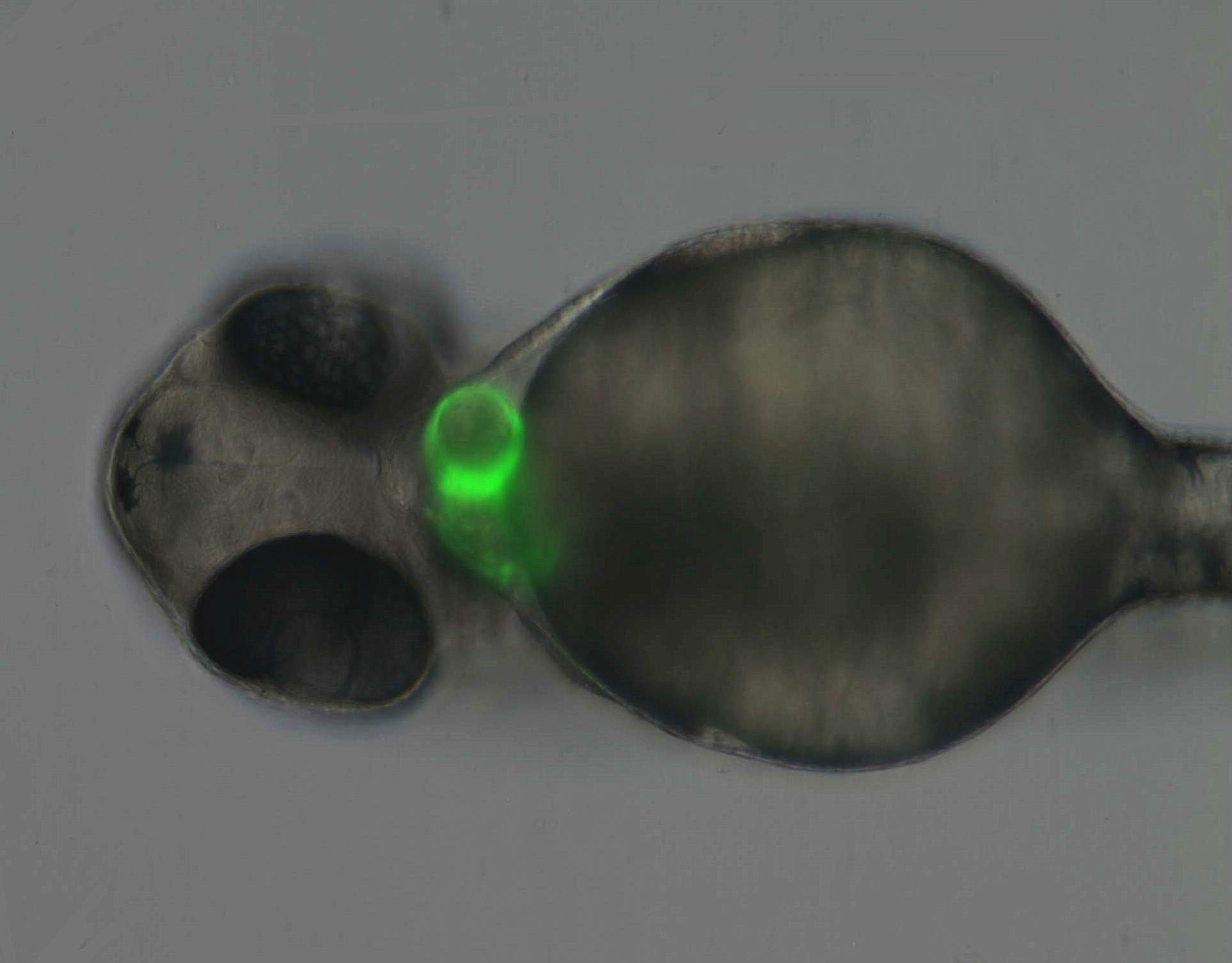
图2 CZ56 (f1Tg, Tg(myl7:eGFP) )
CZ1249 (f2Tg, Tg(-5.1myl7:DsRed2-NLS) )该品系为myl7启动子驱动红色荧光蛋白(DsRed2)在整个心脏肌肉细胞核内表达(图3)[4]。 相比于CZ56,该品系表达荧光蛋白颜色不同且带有核定位信号 。

图3 CZ1249(f2Tg, Tg(-5.1myl7:DsRed2-NLS))
CZ1251 :TgBAC(-36nkx2.5:ZsYellow) 该品系为心脏前体细胞特化的关键转录因子nkx2.5启动子调控黄色荧光蛋白在心管内表达(图4)[5]。 nkx2.5基因为脊椎动物心肌发育中最早表达的转录因子,也是心脏祖细胞的进化保守标记基因 ,与房间隔缺损、室间隔缺损、法络氏四联征、主动脉狭窄等心脏发育缺损相关,在心脏发育中发挥重要作用[6-9]。 该品系对研究心肌细胞分化;心血管细胞的形成及分化具有重要作用。

图4 CZ1251 (TgBAC(-36nkx2.5:ZsYellow))
除了以上心脏特异表达的转基因品系,CZRC还保藏了很多血管特异表达的转基因品系,如 经典的kinase insert domainreceptor like(kdrl,原名flk1)启动子调控多种荧光蛋白在血管特异表达的转基因品系 :CZ62 (s843Tg, Tg(kdrl:EGFP),图5), CZ63 (is5Tg, Tg(kdrl:mCherry),图6) 和CZ70 (la4Tg, Tg(kdrl:RFP))。Kdrl具有蛋白酪氨酸激酶活性,参与循环系统发育和甲状腺发育[10]。kdrl启动子调控的荧光蛋白除在心血管系统之外,在头部、中胚层和腹膜区等细胞中表达[11]。

图5 CZ62 (s843Tg, Tg(kdrl:EGFP))
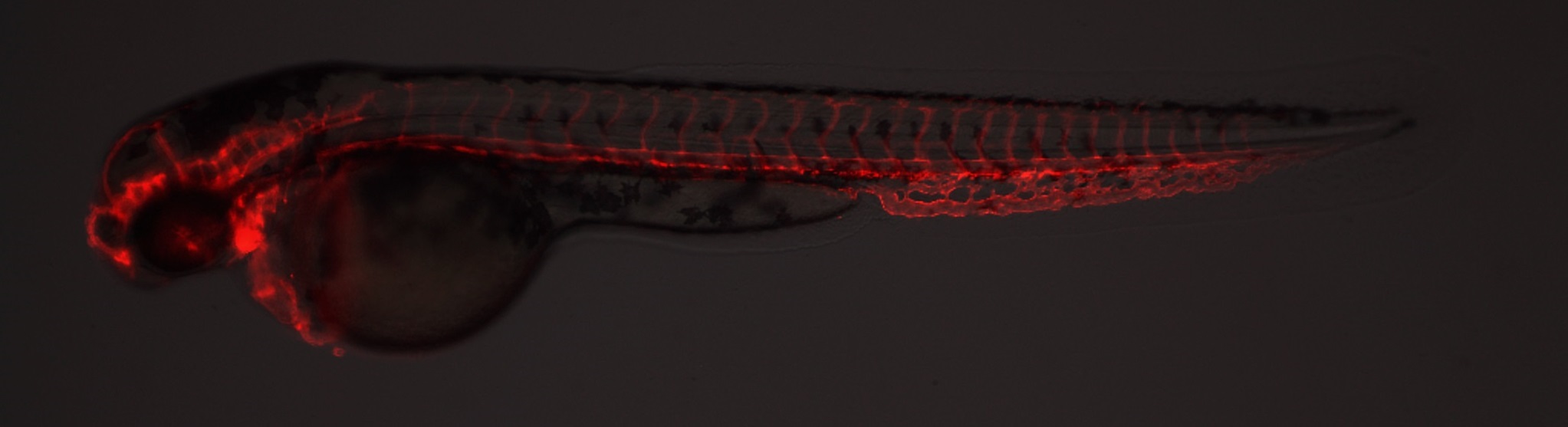
图6 CZ63 (is5Tg, Tg(kdrl:mCherry))
另一常用的心血管系统标记为Fli-1 proto-oncogene, ETS transcription factor a (fli1)启动子调控的转基因品系CZ55 (y1Tg, Tg(fli1:EGFP),图7)和CZ76 (um13Tg, Tg(fli1.ep:DsRedEx),图8),也是常用的血管内皮特异性表达荧光蛋白的转基因品。 相较于kdrl,fli1的表达更广泛,除了血管内皮,还同时标记淋巴管及冠状动脉 [12-14],同时fli1也可标记生血内皮[15]。
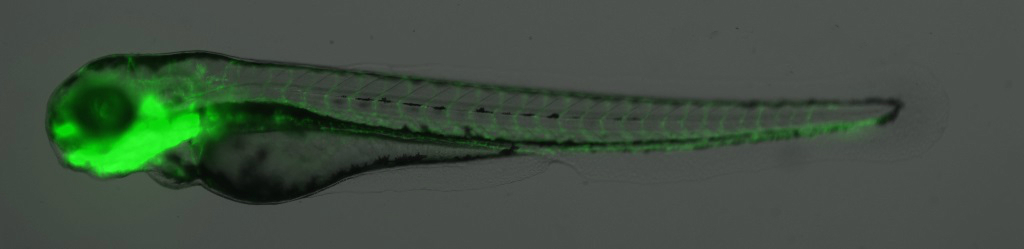
图7 CZ55(y1Tg, Tg(fli1a:EGFP))
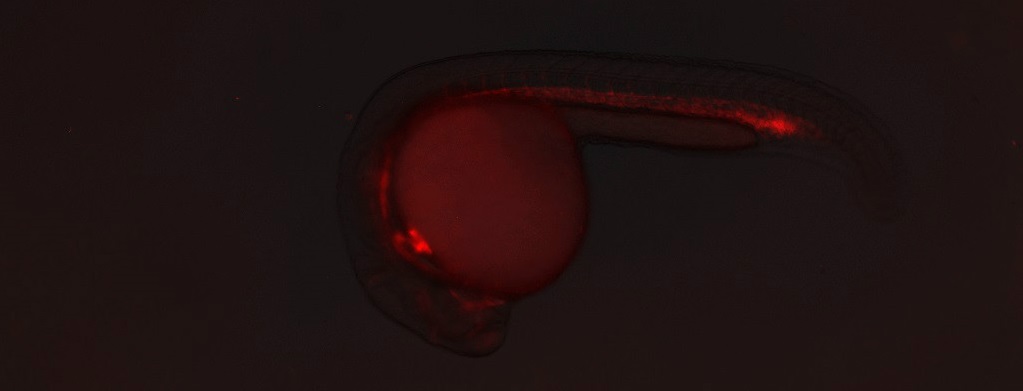
图8 CZ76 (um13Tg, Tg(fli1a.ep:DsRedEx))
除这些常用品系外,CZRC还保藏有另外一些心血管相关标记的品系,有兴趣的研究者可以访问下表提供的链接进行查询。有问题欢迎随时致电或发邮件到CZRC工作邮箱查询。
|
CZ ID |
Genotype |
Construct |
|
ihb6Tg/+ |
Tg(zp3:fsta,myl7:EGFP) |
|
|
y1Tg/+ |
Tg(fli1a:EGFP) |
|
|
f1Tg/+ |
Tg(myl7:GFP) |
|
|
s843Tg/+ |
Tg(kdrl:EGFP) |
|
|
is5Tg/+ |
Tg(kdrl:mCherry) |
|
|
la4Tg/+ |
Tg(kdrl:RFP) |
|
|
um13Tg/+ |
Tg(fli1a.ep:DsRedEx) |
|
|
Tg(hsp:vegf165);Tg(kdrl:GFP) |
Tg(hsp:vegf165);Tg(kdrl:GFP) |
|
|
gd14Tg/+ |
Tg(zp3b:zar1,myl7:EGFP) |
|
|
|
||
|
f2Tg/+ |
Tg(-5.1myl7:DsRed2-NLS) |
|
|
fb7Tg/+ |
TgBAC(-36nkx2.5:ZsYellow) |
1. Bakkers, J., Zebrafish as a model to study cardiac development and human cardiac disease. Cardiovasc Res, 2011. 91(2): 279-88.
2. Hogan BM, Schulte-Merker S. How to Plumb a Pisces: Understanding Vascular Development and Disease Using Zebrafish Embryos. Dev Cell. 2017;42(6):567-583.
3. Burns CG, Milan DJ, Grande EJ, et al.. High-throughput assay for small molecules that modulate zebrafish embryonic heart rate. Nat Chem Biol. 2005;1(5):263-264.
4. Mably JD, Mohideen MA, Burns CG, et al. heart of glass regulates the concentric growth of the heart in zebrafish. Curr Biol. 2003;13(24):2138-2147.
5. Zhou Y, Cashman TJ, Nevis KR, et al. Latent TGF-β binding protein 3 identifies a second heart field in zebrafish. Nature. 2011 May 29;474(7353):645-8.
6. Kim EY, Chen L, Ma Y,et al. Expression of sumoylation deficient Nkx2.5 mutant in Nkx2.5 haploinsufficient mice leads to congenital heart defects. PLoS One. 2011;6(6):e20803.
7. Espinoza-Lewis RA, Liu H, Sun C, et al. Ectopic expression of Nkx2.5 suppresses the formation of the sinoatrial node in mice. Dev Biol. 2011;356(2):359-369.
8. Wang J, Lu Y, Chen H, et al. Investigation of somatic NKX2-5, GATA4 and HAND1 mutations in patients with tetralogy of Fallot. Pathology. 2011;43(4):322-326.
9. Terada R, Warren S, Lu JT,et al. Ablation of Nkx2-5 at mid-embryonic stage results in premature lethality and cardiac malformation. Cardiovasc Res. 2011;91(2):289-299.
10. Liao W, Bisgrove BW, Sawyer H, et al. The zebrafish gene cloche acts upstream of a flk-1 homologue to regulate endothelial cell differentiation. Development. 1997;124(2):381-389.
11. Jin SW, Beis D, Mitchell T, Chen JN, Stainier DY. Cellular and molecular analyses of vascular tube and lumen formation in zebrafish. Development. 2005;132(23):5199-5209.
12. Harrison MR, Bussmann J, Huang Y, et al. Chemokine-guided angiogenesis directs coronary vasculature formation in zebrafish. Dev Cell. 2015;33(4):442-454.
13. Yaniv K, Isogai S, Castranova D, Dye L, Hitomi J, Weinstein BM. Live imaging of lymphatic development in the zebrafish. Nat Med. 2006;12(6):711-716.
14. Lawson ND, Weinstein BM. In vivo imaging of embryonic vascular development using transgenic zebrafish. Dev Biol. 2002;248(2):307-318.
15. Butko E, Distel M, Pouget C, et al. Gata2b is a restricted early regulator of hemogenic endothelium in the zebrafish embryo. Development. 2015;142(6):1050-1061.