西南医科大学张春祥团队建立了促造血药物的高通量虚拟筛选模型
作者:CZRC 发布时间:2023/2/9 3:00:00
血小板减少症是肿瘤患者接受放疗或化疗所产生的主要副作用,亦是新型冠状病毒肺炎(Corona Virus Disease 2019,COVID-19)常见的并发症,更是骨髓移植患者主要的死亡原因之一。然而,暂未发现理想的治疗手段;血小板生成素受体激动剂(TPO receptor agonists,TPO-RAs)广泛应用于多种病因所致的血小板减少症的治疗,但其副作用较大且价格昂贵。此外,TPO-RAs无法用于耐药及血小板生成素受体c-mpl基因缺陷患者的治疗。因此,挖掘TPO-RAs的替代或协同治疗药物是当务之急。TPO/c-MPL是调控巨核细胞分化及血小板生成的主导信号通路,现有研究表明,体内存在非TPO/c-MPL信号途径,对血小板生成亦起到关键的调节作用,但其分子调控网络远未阐明。


近日,西南医科大学张春祥教授团队于血液学领域权威杂志Haematologica上在线发表了题为“Targeting TPO-independent strategy in the discovery of a novel megakaryocytopoiesis inducer DMAG for treatment of thrombocytopenia”的研究论文。该研究利用一种最新的深度学习算法:Multi-Grained Cascade Forest(gcForest)首次建立了促造血药物的高通量虚拟筛选模型,通过该模型从化合物库中筛选出来源于中药地榆的天然产物3,4'-O-二甲基逆没食子酸-4-O-α-D-葡萄糖苷(3,4'-O--dimethylellagic acid-4-O-α-D-glucoside,DMAG)具有潜在活性。通过细胞、血小板减少症小鼠、c-mpl基因敲除(c-MPL-/-)小鼠,以及Tg(cd41:eGFP)转基因斑马鱼模型证明DMAG显著促进巨核细胞分化及血小板生成,对血小板减少症具有良好的治疗作用,并证明DMAG通过非TPO/c-MPL依赖的ERK/HIF1/NF-E2信号通路促进巨核细胞分化及血小板生成(图1)。
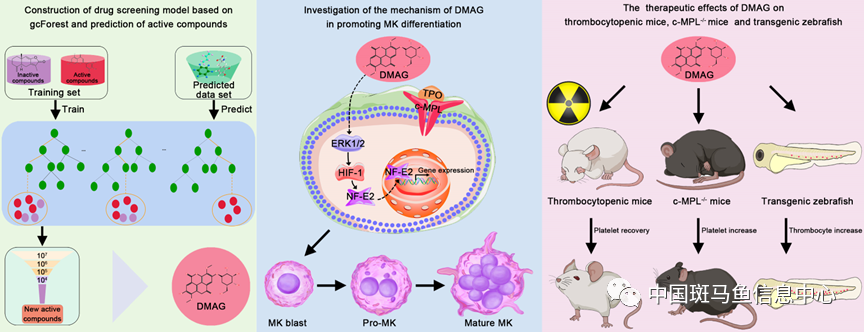
图1 图形摘要

图1 图形摘要
由于传统实验室药物发现成本高、效率低,迫切需要一种虚拟药物筛选模型,对海量化合物进行高通量筛选。该研究首先通过一种最新的深度学习算法gcForest建立了促造血药物筛选模型(图2),对化合物库进行活性筛选,发现天然化合物DMAG具有高活性。
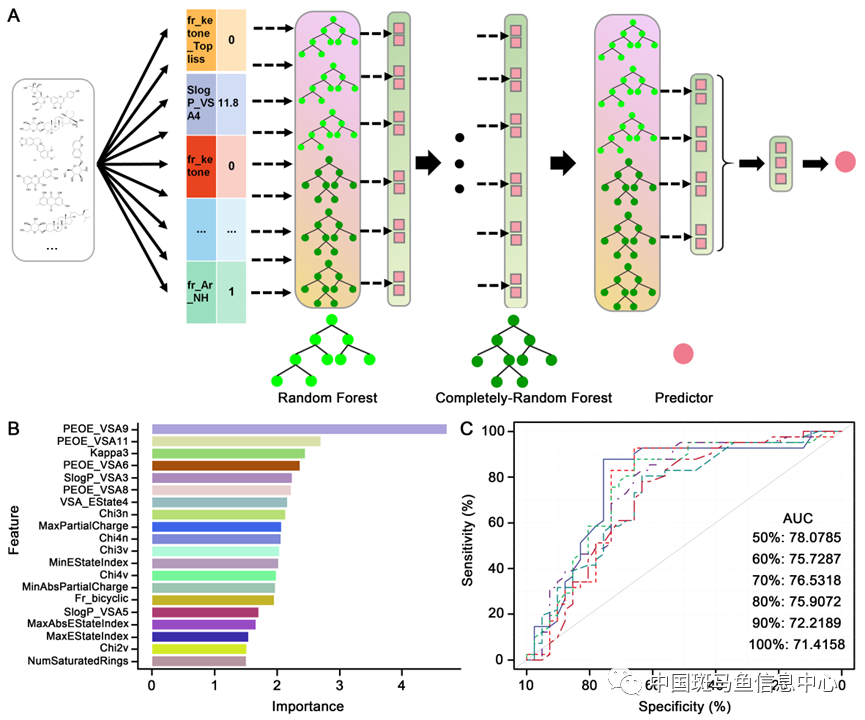
图2 药物筛选模型构建

图2 药物筛选模型构建
研究人员通过K562和Meg-01细胞、辐照诱导的血小板减少症小鼠、CRISPR/Cas9构建的c-MPL-/-小鼠,在体内外研究了DMAG的药物活性,结果发现DMAG显著诱导K562和Meg-01细胞向巨核细胞分化,促进血小板减少症小鼠血小板水平恢复、巨核细胞生成和分化、血小板生成及激活,并提升c-MPL-/-小鼠的血小板水平。利用Tg(cd41:eGFP)转基因斑马鱼模型,证明不同浓度的DMAG能明显促进斑马鱼体内的血小板生成(图3)。
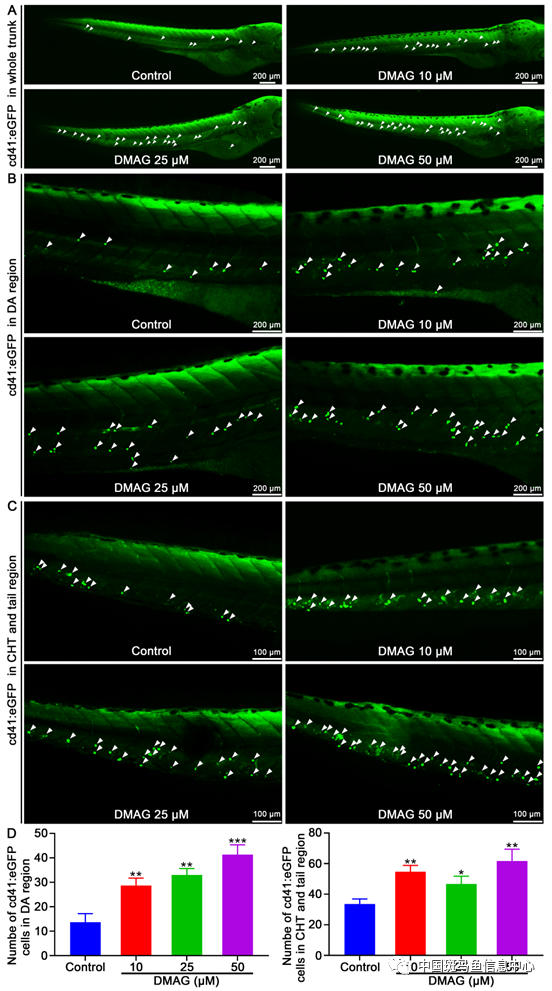
图3 DMAG促进斑马鱼血小板生成

图3 DMAG促进斑马鱼血小板生成
研究人员进一步通过RNA sequencing技术探究了DMAG促进巨核细胞分化的基因表达谱,并通过信号通路分步阻断策略验证了DMAG调控的信号通路,发现DMAG通过激活ERK/HIF1/NF-E2信号通路促进巨核细胞分化,从而加强血小板生成,且该药物作用不依赖于TPO/c-MPL经典信号通路(图4)。
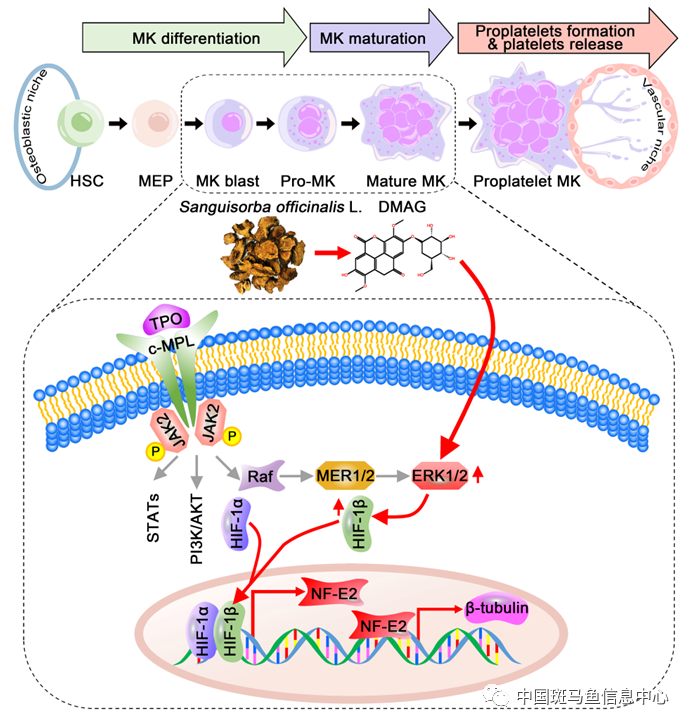
图4 DMAG调控巨核细胞分化及血小板生成的作用机制

图4 DMAG调控巨核细胞分化及血小板生成的作用机制
综上,该研究首次基于深度学习算法建立了一种高效精准的促造血药物筛选模型,发现了一种来源于中药地榆的天然化合物DMAG具有良好的血小板减少症治疗作用,并挖掘出一条非TPO/c-MPL依赖的ERK/HIF1/NF-E2信号通路可调控巨核细胞分化及血小板生成。该研究为DMAG的临床转化提供了理论依据,为新药研发提供了一种有效策略,并进一步完善了巨核细胞分化及血小板生成的分子调控网络。
西南医科大学王龙副教授、罗杰斯副教授和刘莎老师为该论文第一作者,张春祥教授、吴建明教授和吴安国副教授为该论文通讯作者。该研究得到了国家自然科学基金、四川省杰出青年科学基金的资助。