刘峰团队揭示胚胎期造血干祖细胞铁死亡机制
作者:CZRC 发布时间:2023/6/2 9:00:00
脊椎动物造血发育过程分为初级造血和次级造血两个阶段,初级造血主要产生初级髓系和红系细胞,次级造血主要产生造血干祖细胞。其中,初级血细胞作为重要的微环境细胞组分,在多个层面参与造血干祖细胞发育的调控[1]。比如,初级髓系细胞能通过分泌炎性信号[2]、降解胞外基质[3]等促进造血干祖细胞产生。但是,初级红细胞在生理或病理状态下对造血干祖细胞产生的影响尚不明确。哺乳动物中,初级红细胞缺陷突变体由于胚胎缺氧而致死,胚胎不能存活至次级造血阶段[4]。而斑马鱼胚胎在体外发育,发育早期可以通过渗透作用吸收氧气,因此斑马鱼初级红细胞缺陷的胚胎可以存活至次级造血阶段[5, 6]。此外,红细胞发生和铁代谢密切相关。近年研究表明,骨髓微环境中铁的浓度能影响造血干细胞命运决定[7],特定病理状态下的造血干细胞也对铁死亡敏感[8]。然而,胚胎发育过程中,铁稳态是否影响造血干祖细胞的产生也仍不清楚。
近期,中国科学院动物研究所刘峰研究组在Development杂志上发表了题为“Heme-deficient primitive red blood cells induce HSPC ferroptosis by altering iron homeostasis during zebrafish embryogenesis”的研究论文。在这篇文章中,研究人员揭示了血红素缺陷初级红细胞导致造血干祖细胞铁死亡的调控机制。


首先,研究人员使用反义寡核苷酸(Morpholino)基因敲降技术构建了斑马鱼初级红细胞发育缺陷模型,筛选后发现只有在敲低红细胞血红素合成限速酶编码基因alas2和alad的斑马鱼胚胎中出现造血干祖细胞缺陷表型。随后在功能缺失突变体中证实了造血干祖细胞缺陷的表型。进一步研究发现,alas2和alad缺陷的胚胎中,红细胞数目不受影响,但血红蛋白缺失,机体铁代谢异常,红细胞出现铁聚集的表型。
随后,研究人员通过检测血清铁含量,证实了血红素缺陷的异常红细胞会导致血液铁过载。分选红细胞进行转录组测序分析,以及抑制剂处理实验进一步证实了异常初级红细胞通过铁转运蛋白(Slc40a1)介导铁的外排,导致血液铁过载。而血液铁过载和造血干祖细胞缺陷密切相关。通过使用gata1 morpholino注射的方式,阻碍突变体中初级红细胞的产生,不仅能恢复血液铁水平,还能回救造血干祖细胞缺陷表型。进一步证实了异常初级红细胞引起的血液铁过载是导致造血干祖细胞缺陷的重要因素。
上述结果提示,造血干祖细胞的数目减少可能与铁死亡相关。研究人员通过扫描电镜成像,发现alas2和alad突变体中,造血干祖细胞呈现出明显的铁死亡特征改变,包括线粒体形态变化、细胞质膜的破坏等(图1)。进一步检测发现alas2和alad突变体中造血干祖细胞促铁死亡相关的大分子氧化酶编码基因表达量升高,抗铁死亡相关蛋白(包括Fth1、Gpx4和Slc7a11)含量减少。除此之外,研究人员使用铁螯合剂(DFO)以及铁死亡抑制剂(Ferrostatin-1)处理都能有效回救造血干祖细胞缺陷的表型。以上结果表明,alas2和alad突变体中造血干祖细胞发生了铁死亡。
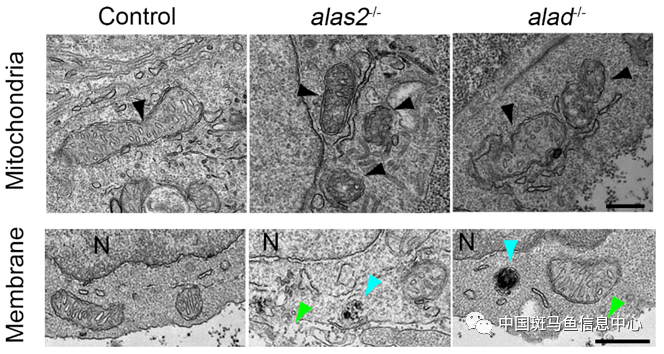
图1 alas2和alad突变体中造血干祖细胞出现明显铁死亡特征表型

图1 alas2和alad突变体中造血干祖细胞出现明显铁死亡特征表型
此外,进一步功能实验证实了造血干祖细胞通过转铁蛋白受体(Tfr1b)响应铁过载环境,导致过量铁的摄入。氧化应激相关检测表明,过量铁引起造血干祖细胞活性氧水平升高,细胞氧化应激压力升高。结合脂质氧化组学检测,证实了花生四烯酸类脂质过氧化是导致造血干祖细胞铁死亡的直接原因。最后,研究人员通过造血干祖细胞移植实验,初步明确了受铁死亡影响的主要为红系倾向性的造血干祖细胞。
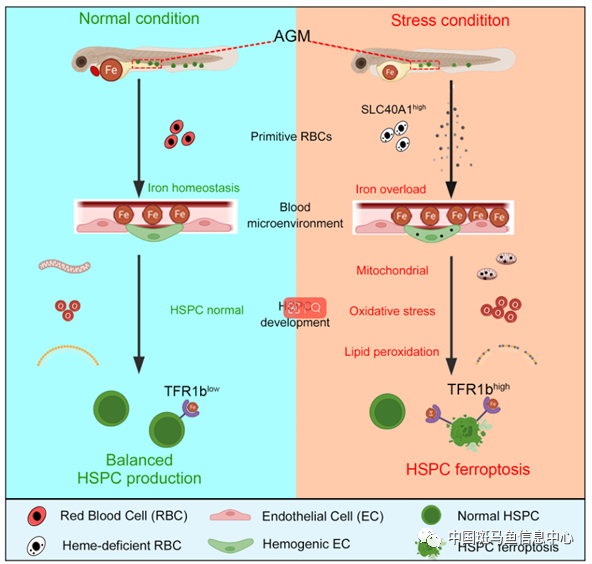
图2 工作模式图

图2 工作模式图
综上所述,这项研究发现,在alas2和alad突变体中,血红素缺陷的初级红细胞导致造血干祖细胞铁死亡。机制上,异常红细胞通过Slc40a1导致血液铁过载,而造血干祖细胞Tfr1b介导了过量铁的摄入,进而通过铁-活性氧-脂质氧化轴介导了造血干祖细胞的铁死亡(图2)。该研究揭示了红细胞铁稳态在造血干祖细胞发育过程中的重要作用,为铁代谢异常导致的恶性血液疾病提供了潜在的临床指导。
参考文献:
1. Vink, C.S., S.A. Mariani, and E. Dzierzak, Embryonic Origins of the Hematopoietic System: Hierarchies and Heterogeneity.Hemasphere, 2022. 6(6): p. e737.
2. Espin-Palazon, R., et al., Proinflammatory signaling regulates hematopoietic stem cell emergence. Cell, 2014. 159(5): p. 1070-1085.
3. Travnickova, J., et al., Primitive macrophages control HSPC mobilization and definitive haematopoiesis. Nat Commun, 2015. 6: p. 6227.
4. Baron, M.H., J. Isern, and S.T. Fraser, The embryonic origins of erythropoiesis in mammals. Blood, 2012. 119(21): p. 4828-37.
5. Lyons, S.E., et al., A nonsense mutation in zebrafish gata1 causes the bloodless phenotype in vlad tepes. Proc Natl Acad Sci U S A, 2002. 99(8): p. 5454-9.
6. Ransom, D.G., et al., The zebrafish moonshine gene encodes transcriptional intermediary factor 1gamma, an essential regulator of hematopoiesis. PLoS Biol, 2004. 2(8): p. E237.
7. Zhang, D., et al., The microbiota regulates hematopoietic stem cell fate decisions by controlling iron availability in bone marrow. Cell Stem Cell, 2022. 29(2): p. 232-247 e7.
8. Zhao, J., et al., Human hematopoietic stem cell vulnerability to ferroptosis. Cell, 2023. 186(4): p. 732-747 e16.